ALS治療薬を承認申請 特定の遺伝子変異が対象
米製薬企業バイオジェン日本法人は21日、筋萎縮性側索硬化症(ALS)の治療薬「トフェルセン」の製造販売の承認を厚生労働省に申請したと発表した。SOD1と呼ばれる遺伝子に変異のある患者を対象とした薬で患者の約2%を占める。
バイオジェンによると、臨床試験では28週間後時点で神経の損傷を示す血中物質が減少。症状の進行を抑えると期待されている。米食品医薬品局(FDA)は2023年4月に迅速承認した。
ALSは筋肉の運動に関する神経細胞が侵される難病で、徐々に体を動かせなくなる。国内のALS患者数は推定約1万人。
RECOMMEND
あなたにおすすめPICK UP
注目コンテンツNEWS LIST
全国のニュース 「医療」記事一覧-
外来診療混雑、感染対策を インフル報告最多で厚労相
共同通信
-
沢井、タミフル後発薬の供給停止 インフル流行で製造追いつかず
共同通信
-
「インシデント隠蔽」投稿 千葉大病院看護師か、内部調査
共同通信
-
呼吸器感染「予想の範囲」 中国の状況にWHO
共同通信
-
米国で鳥インフルエンザ初の死者 南部ルイジアナ州で、高齢の患者
共同通信
-
中国、呼吸器感染症が拡大 インドでも確認、ベトナムは注視
共同通信
-
付き添い入院、寝具費を補助 親負担軽減へ初の支援策
共同通信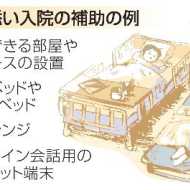
-
酒に「がんのリスク」表示を 米国の医務総監が勧奨
共同通信
-
WHO、中国にデータ共有要請 コロナ起源巡り
共同通信
-
中国、コロナ初確認から5年 不満募る武漢、米中対立再燃も
共同通信