後発薬4割、承認書と異なる製造 業界自主点検に「衝撃的」

日本製薬団体連合会(日薬連)は21日までに、ジェネリック医薬品(後発薬)を扱う全172社が実施した製造実態に関する自主点検の結果、8734品目中、4割超に当たる3796品目で製造販売承認書と異なる製造があったと明らかにした。厚生労働省の会議で速報値として報告し「品質や安全性に影響はない」としたが、会議構成員からは「衝撃的な数字だ」として再発防止を強く求める声が上がった。
処方薬全体の約8割を占める後発薬を巡っては品質不正が相次ぎ発覚し、2021年以降、小林化工(福井県あわら市)や大手の日医工(富山市)など21社が業務停止などの行政処分を受けた。医薬品供給不足の一因にもなり、不適切事案の発生防止のため厚労省が自主点検を求めていた。
日薬連によると、点検では書類確認や従業員のヒアリングをし、製造販売承認書と異なる方法で原材料を混合したり、品質試験を行ったりといった事例が判明した。承認書の誤記もあった。品質や安全性に問題がある「重大な相違」の事例はなかったという。
RECOMMEND
あなたにおすすめPICK UP
注目コンテンツNEWS LIST
全国のニュース 「医療」記事一覧-
遠方への妊婦健診、交通費を補助 8割分、リスクある人ら対象
共同通信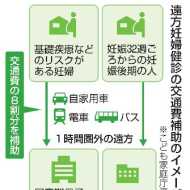
-
高額療養負担上限25年8月上げ 26年度からは年収区分細分化
共同通信
-
二大バイオバンク連携強化 患者と健常者の比較容易に
共同通信
-
人の培養血管製品を初承認 米FDA、重傷者に移植
共同通信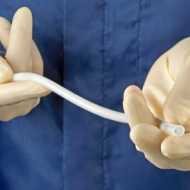
-
薬価、一律引き下げ見直し 政府、2500億円抑制へ
共同通信
-
在宅医療患者1日23万人で最多 23年調査、入院は最少更新
共同通信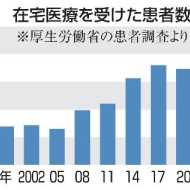
-
インフル流行「注意報レベル」 前週比2倍超、全国で増
共同通信
-
コロナ感染者3週連続増 前週比1・27倍、厚労省発表
共同通信
-
内密出産「慎重に議論」 三原こども担当相
共同通信
-
電子処方箋トラブルで点検 24日まで発行停止
共同通信





















